La vision des oiseaux – un monde à découvrir
Pourquoi s’intéresser à la vision des oiseaux ?
L’acuité visuelle de l’aigle ou de l’hirondelle fondant sur sa proie et la capturant en plein vol est digne d’émerveillement. La plupart des oiseaux dit modernes, ou Neoaves, ont une vision de qualité similaire voire même, pour certaines espèces, supérieure à la nôtre.
L’œil des oiseaux peut nous aider à mieux comprendre comment le nôtre est construit et comment il fonctionne. Il offre également une occasion de nous interroger sur les causes de maladies de l’œil, comme le glaucome ou la dégénérescence maculaire liée à l’âge (DMLA).

En apprendre plus sur la vision des oiseaux
La vision des oiseaux est très performante
Les performances visuelles dépendent de quatre propriétés distinctes : 1) perception nette d’une image (ou acuité visuelle), 2) perception des couleurs, 3) perception des mouvements (vitesse, orientation, direction), 4) sensibilité à la lumière. Les deux premières propriétés sont, chez les primates, bien supérieures à celles des autres mammifères, mais similaires à celles des oiseaux modernes. Par contre, des oiseaux comme les passereaux, rapaces ou colombinés sont mieux équipés que les primates pour détecter les mouvements rapides.

Pourquoi la vision diurne des oiseaux et celle des primates est sans égal dans le monde animal ?
Sur la base de nos connaissances actuelles, on pense que c’est en grande partie lié à la présence d’une région spécialisée de la rétine qui s’appelle la fovéa. Chez les mammifères, seuls les primates ont une fovéa. Bien que les rétines de moins d’une centaine d’espèces d’oiseaux (1% du nombre total d’espèces) aient été étudiées à ce jour, on pense que la grande majorité des Neoaves diurnes ont une voire deux fovéas. Par contre, les oiseaux dits anciens comme les poules, les canards ou les oies en sont privés. L’apparition de la fovéa chez les oiseaux au cours de l’évolution a permis, entre autres, d’améliorer la précision et la vitesse du vol.
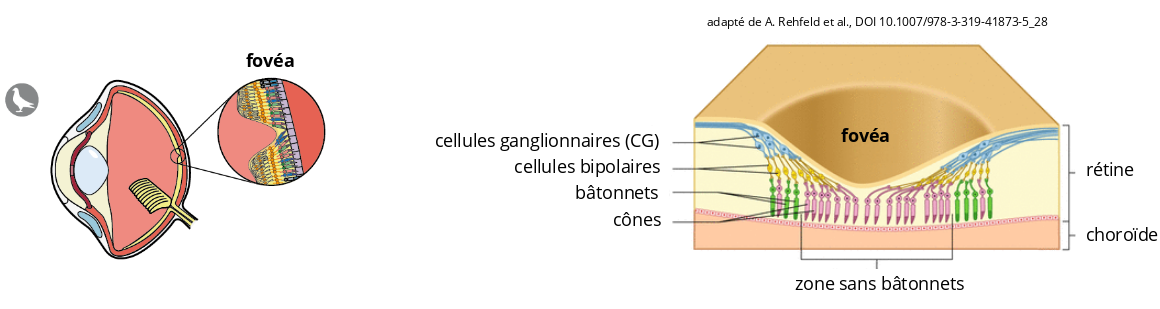
Qu’est-ce que la fovéa ?
La fovéa est une région spécialisée de la rétine. C’est grâce à cette structure, aux propriétés très particulières, que des images projetées sur la rétine sont perçues par le cerveau avec une grande netteté et en couleur.

Transduction du signal lumineux au niveau de la fovéa
Dans la rétine, les photorécepteurs (cônes et bâtonnets) transforment les signaux lumineux en signaux électriques et chimiques qui sont ensuite transmis aux cellules ganglionnaires (CG). Ce sont ces neurones rétiniens qui transmettent, via le nerf optique, l’information vers différentes régions du cerveau.

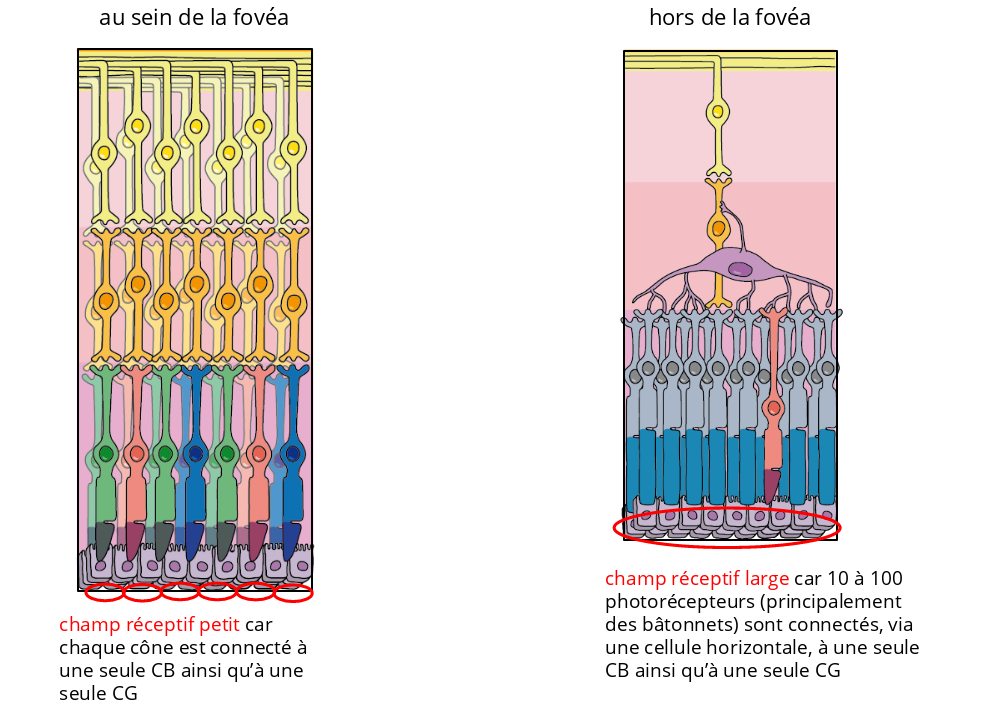
Pourquoi la fovéa a-t-elle des propriétés exceptionnelles ?
Chez les espèces dotées d’une fovéa (oiseaux modernes et primates), chaque CG reçoit des signaux générés par un seul cône. En revanche, chez les espèces sans fovéa une seule et unique CG récolte les signaux d’un grand nombre de bâtonnets qui définissent le champ récepteur de cette CG. Le champ récepteur d’une CG localisée dans la fovéa est par conséquent beaucoup plus petit que celui d’une CG située hors de la fovéa. Il y a une analogie entre la taille du champ récepteur d’une CG et celle d’un pixel d’une image numérique. En effet, plus les pixels qui composent une image numérique sont petits, meilleure est la qualité de cette image. C’est ainsi qu’une image transmise au cerveau par la fovéa sera perçue avec une plus grande netteté que celle transmise par une rétine sans fovéa.
La fovéa, moteur de l’évolution ?
Les analyses génomiques récentes suggèrent que les oiseaux modernes, ou Neoaves, se sont séparés de leurs ancêtres, les Galloanserae, au moment de l’extinction Crétacé-Paléogène, il y a de cela 66 millions d’années. Cette branche évolutive des oiseaux a eu un tel succès que plusieurs milliers de nouvelles espèces sont apparues durant une période relativement brève. Ces oiseaux modernes ont colonisé les terres et les mers sous toutes les latitudes. On ne connait pas l’élément déclencheur à l’origine de ce succès. Une hypothèse que nous avançons serait une perception visuelle plus performante, avec notamment l’apparition d’une ou deux fovéas dans leur rétine. Une augmentation marquée de l’acuité visuelle a sans doute permis d’améliorer la qualité de leur vol qui est devenu plus rapide, précis et soutenu. La conquête du ciel par la plupart des Neoaves a eu des conséquences majeures sur leur métabolisme qui s’est accéléré, et a favorisé le développement d’un corps plus léger avec un squelette constitué d’os creux. L’amélioration du vol et l’augmentation de l’acuité visuelle ont aussi favorisé des changements de régimes alimentaires. Alors que les Galloanserae sont végétariens et se nourrissent au sol, les Neoaves attrapent souvent des proies vivantes comme des insectes, des crustacés, des vers et parfois de petits vertébrés.

Nos travaux nous ont permis de découvrir que la présence d’une fovéa dans la rétine s’accompagne de changements importants, non seulement au niveau de l’organisation de la rétine, mais également de celle de certaines régions du cerveau. Un sérieux problème qu’ont dû rencontrer les Neoaves au cours de leur évolution a été l’allongement de leur développement rendu nécessaire par les perfectionnements au niveau de la rétine et du cerveau. Contrairement aux oisillons des Galloanserae qui sont autonomes immédiatement après l’éclosion et quittent rapidement le nid, les oisillons des Neoaves naissent souvent avec les yeux fermés et sont pris en charge par leurs parents pendant plusieurs semaines. Ce passage d’un mode de développement précoce à un développement qui se prolonge au-delà de l’éclosion, a nécessité des changements de comportement spectaculaires. En outre, le séjour prolongé des oisillons au nid a donné du temps au cerveau pour qu’il développe des fonctionnalités nouvelles. En un mot, les Neoaves sont devenus plus intelligents que leurs ancêtres.
Pourquoi s’intéresser à la fovéa ?
Avec des densités de neurones très élevées et une activité métabolique intense, la fovéa est l’une des régions les plus sollicitées de notre système nerveux. Chez l’Homme, la fovéa ainsi que la rétine qui l’entoure, appelée macula, peuvent être la cible de maladies de la rétine comme la tristement célèbre dégénérescence maculaire liée à l’âge (DMLA). Cette maladie neurodégénérative touche un nombre croissant de nos concitoyens. L’importance de la fovéa pour la vision et sa susceptibilité aux maladies de l’œil doivent nous inciter à intensifier la recherche dans ce domaine.
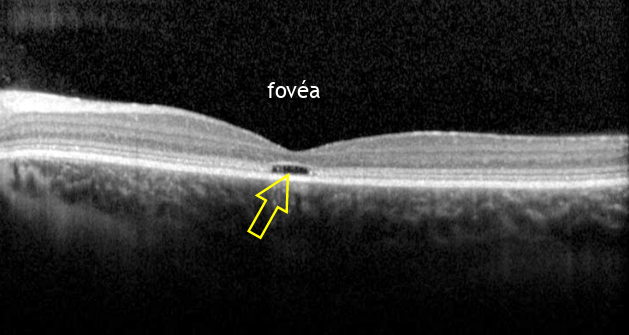
Exemple de maladie de l’œil : une dystrophie maculaire
Une dystrophie de la fovéa d’origine génétique met en évidence le caractère singulier de cette zone de la rétine. Les auteurs dans Vaclavik et al., 2013 ont décrit deux cas chez des patients atteints d’une maladie neurodégénérative appelée ataxie spinocérébelleuse (SCA) et associée à une perte de vision (acuité et couleurs). Cette maladie est provoquée par le gène sca1 qui porte une mutation et code pour une protéine anormale appelée ATXN1. Chez ces patients, une cavité se forme au niveau de leur fovéa. Cette cavité résulte de la perte des cônes.
Projets de recherche en cours
La fovéa chez l’humain et les oiseaux a été découverte à la fin du 19ème siècle, mais les études sporadiques qui ont suivi n’ont pas permis d’avancées significatives des connaissances. Ceci est lié au fait que les recherches dans le domaine de la vision sont menées, en priorité, chez la souris et le poisson zèbre, deux espèces qui n’ont pas de fovéa. Les primates non-humains seraient en théorie les meilleurs modèles pour étudier la fovéa, mais leur accès à l’expérimentation est limité pour des raisons éthiques évidentes. Récemment, le développement d’organoïdes qui reproduisent in vitro la micro-anatomie d’un organe comme l’œil suscite beaucoup d’intérêt. Malheureusement, les recherches conduites jusqu’à ce jour n’ont pas permis d’observer le développement d’une fovéa dans les cultures d’organoïdes rétiniens dérivés de cellules souches pluripotentes humaines.
Actuellement, trois projets de recherche soutenus par la Fondation Gene&Vision sont en cours :
Articles

Conférence de Jean-Marc Matter à L'Université de Californie, Irvine
(en anglais)

Voici notre dernière publication qui vient de paraître dans la revue scientifique "Developmental Biology"
(en anglais)
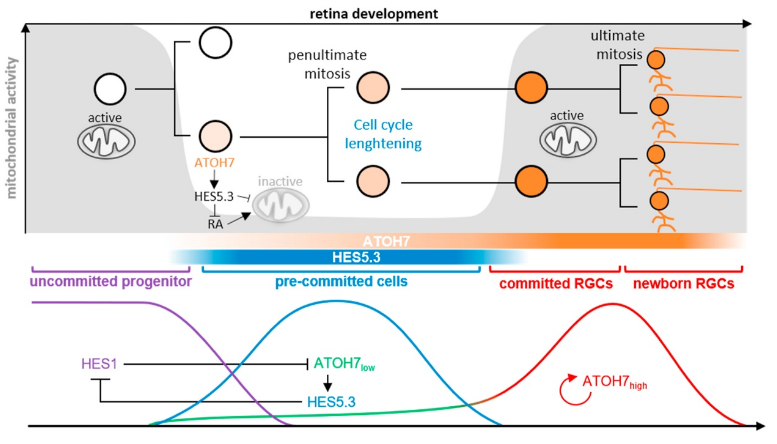
Une publication parue dans la revue scientifique "Developmental Biology"
(en anglais)
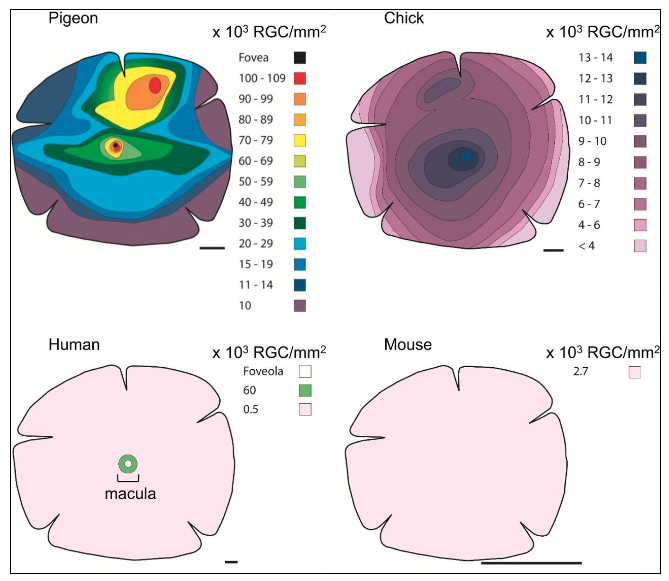
Une publication parue dans la revue scientifique "Development"
(en anglais)